개요
의료기기 수입업자는 한국의료기기산업협회장에게 전자문서교환방식 등에 의한 표준통관예정보고를 필 한 후 통관하여야 한다.
다만, 다운로드 받는 소프트웨어 의료기기 등 식품의약품안전처장이 지정 공고하는 소프트웨어 의료기기(SaMD)는 제외한다.
[참고]
의료기기란?
"의료기기"란 사람이나 동물에게 단독 또는 조합하여 사용되는 기구·기계·장치·재료·소프트웨어 또는 이와 유사한 제품으로 다음 각 호의 어느 하나에 해당하는 제품을 말한다.
(다만, 약사법에 따른 의약품과 의약외품 및 장애인복지법 제65조에 따른 장애인보조기구 중 의지·보조기는 제외한다.)
좌우로 움직여보세요
| 호 | 의료기기 |
|---|---|
| 1 | 질병을 진단ㆍ치료ㆍ경감ㆍ처치 또는 예방할 목적으로 사용되는 제품 |
| 2 | 상해(傷害) 또는 장애를 진단ㆍ치료ㆍ경감 또는 보정할 목적으로 사용되는 제품 |
| 3 | 구조 또는 기능을 검사ㆍ대체 또는 변형할 목적으로 사용되는 제품 |
| 4 | 임신을 조절할 목적으로 사용되는 제품 |
의료기기 해당여부 확인
좌우로 움직여보세요
| 번호 | 방법 / 예시 |
|---|---|
| 1 |
의료기기전자민원창구 홈페이지 > 상단의 민원신청 > 전자민원안내 및 신청을 클릭
|
| 2 |
민원사무 검색창에 '의료기기질의' 검색 및 '의료기기질의' 항목 클릭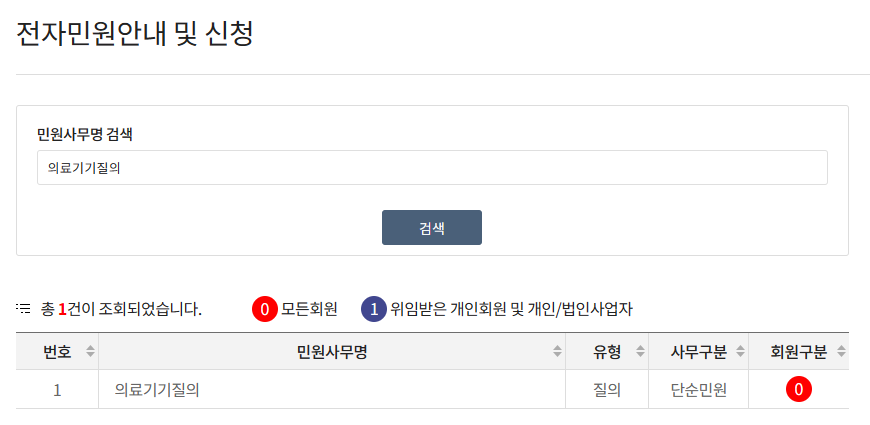
|
| 3 |
민원설명(구분, 민원사무분류, 처리부서, 수수료, 처리일자), 민원개요, 관련법규 참조 및 구비 서류를 지참하여 민원신청 버튼을 클릭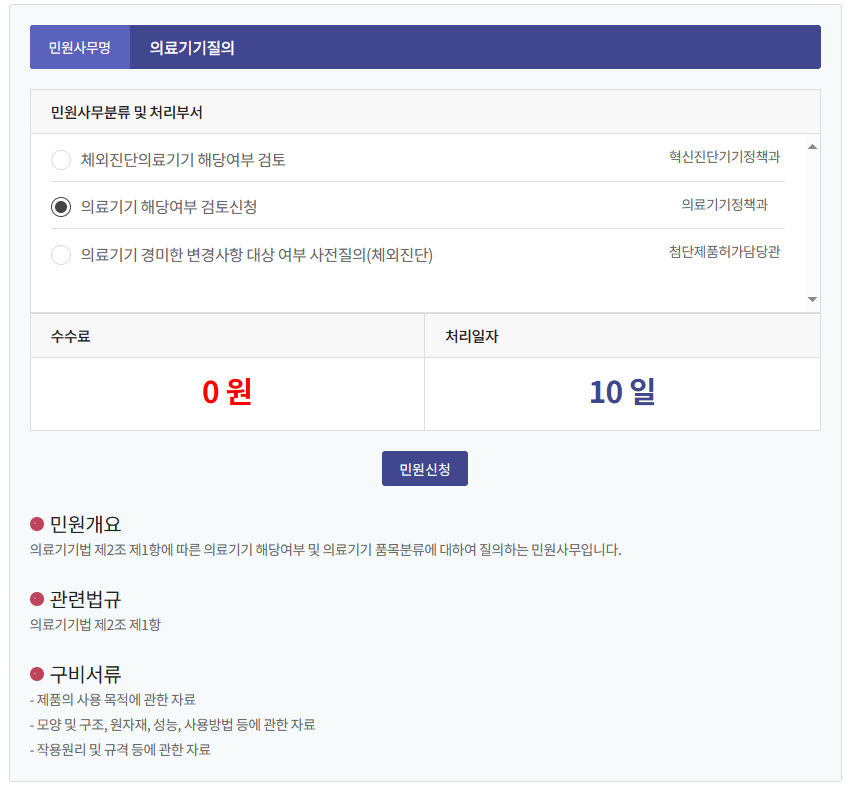
|
** 의료기기안심책방 홈페이지 주소: https://emedi.mfds.go.kr/
** 의료기기 해당 시, 표준통관예정보고 발급 필수
수입자 자격요건
좌우로 움직여보세요
| 수입자 | 위탁자 | 구비서류 | |
|---|---|---|---|
| 의료기기,체외진단의료기기 |
|
|
|
의료기기 수입절차
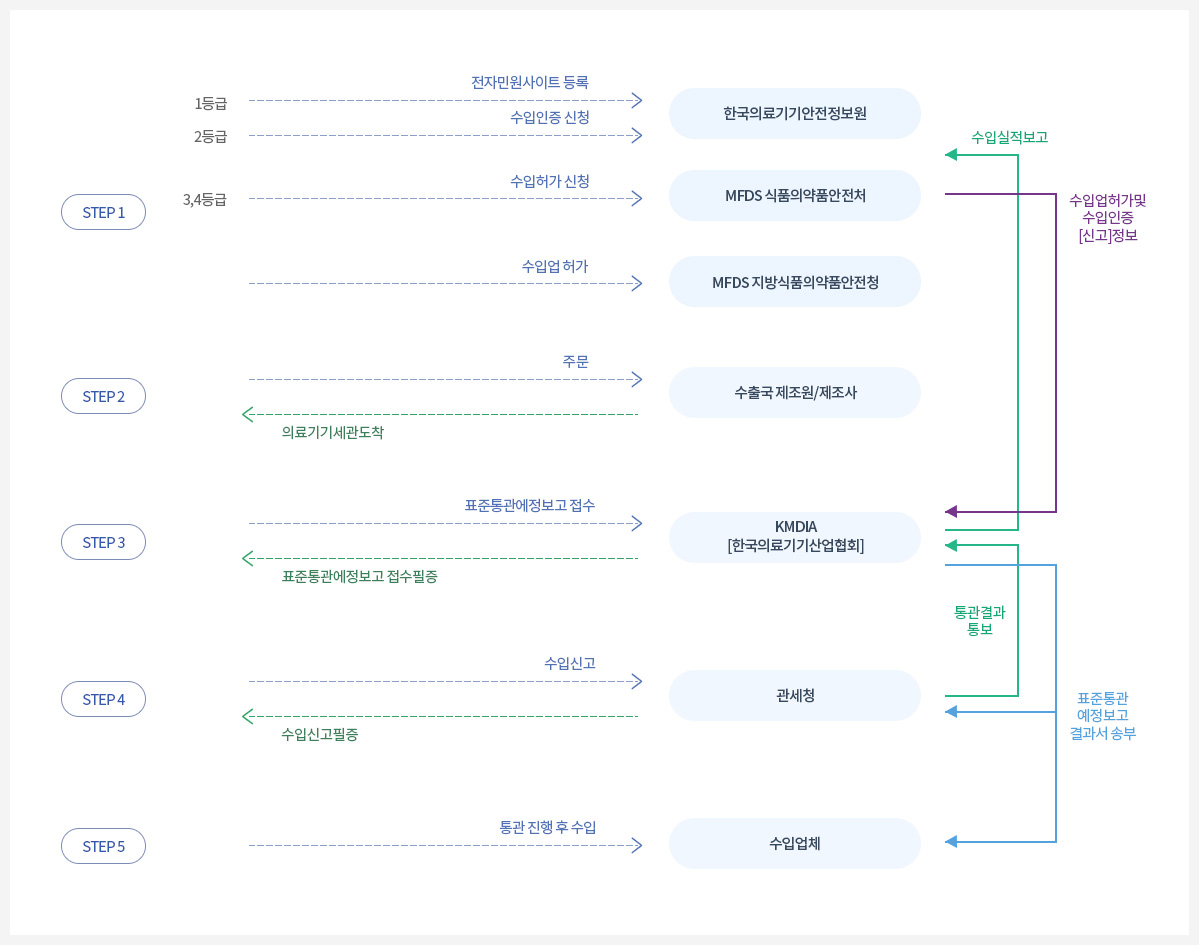
[의료기기수입절차 행정처분 관련사항 안내 공문]
표준통관예정보고 처리 절차
- step 01.전자문서 신규개통
- step 02.확인서류 검토 및 신규업체등록(※최초 1회만 제출)
- step 03.신규개통 완료
- step 04.품목 DB 검토(※모델명 10개 이하시 생략)
- step 05.표준통관예정보고 접수
- step 06.표준통관예정보고 검토
- step 07.승인/오류통보
- step 08.표준통관예정보고 접수필증(승인문서)
- step 09.전자 세금계산서 발행
step 01
step 03
step 08
- 관세청 및 ASP서비스 제공업체에 이용 신청
- 사업자등록증
- 의료기기 수입업허가증
- 품목DB
step 03
- 수입업체에 품목DB 송부 및 신규 개통 완료 알림
- 수입허가/인증(신고)증과 품목 DB 일치 여부 검토 ※모델명이 10개 이상인 경우만 제출함
- 검토 완료된 품목DB를 협회 시스템에 업로드함
- 관세청 및 ASP서비스 제공업체 사이트에서 전자문서(XML)로 송신
- 수입 허가/인증(신고) 사항 검토
- - 수신된 품목사항과 협회 DB 일치 여부 확인
- - 식품의약품안전처 품목대장(협업 시스템)활용
- 시험용의료기기등확인서 및 임상시험계획 승인서 등 확인 검토
- 처리기한
- - 접수 후 업무처리 시간 기준 8시간 이내
- - BSE 서류 제출 건은 업무처리 시간 기준 3일 이내 (단, 보완(오류) 통보 후 재접수 된 건은 재접수된 시점으로부터 업무처리 시간 기준 8시간 이내)
[수입요건확인 강화 사항]
- - BSE(TSE) 관련 사항
- - 치과용비귀금속합금 관련 사항
- - 모유착유기 관련품목 수입
- - 안전성·유효성 문제 원자재 사용 의료기기(수은(치과용제외), ‘DEHP, DBP, BBP’ 함유 수액세트, 분말 함유 장갑, 석면 등)
step 08
- 관세청 및 수입업체에 승인 문서 전송
- 표준통관예정보고서 관련 세금계산서 발행(월1회)
표준통관예정보고 작성방법 안내
문의
좌우로 움직여보세요
| 구분 | 담당자 | 연락처 | 메일 |
|---|---|---|---|
| 민원 교육 및 의료기기 통관 관련 규정 제조원·수출자 검토 |
조은비 팀장 | 02-596-0786 | import@kmdia.or.kr |
| 수입요건강화사항관련 (BSE, 모유착유기, 베릴륨 등) |
설정빈 과장 | 02-596-7479 | |
| 수입요건 확인면제(대외무역법) | 박해주 대리 | 02-596-7470 | |
| 품목DB검토 및 변경 | 김성빈 팀원 | 070-7725-0252 | |
| 수입요건 확인면제(임상용 의료기기) 세금계산서 |
김원섭 팀원 | 02-596-7769 | |
| 수입요건 확인면제 (시험용의료기기등 의료기기법) 신규개통 및 수입•통관절차 안내 |
이송연 팀원 | 02-596-7491 | |
| 관세청 파견 | 윤효상 과장, 박경빈 팀원 |

 파일다운로드[공문]
파일다운로드[공문]